人體研究計畫審查費收費標準
發布日期 :
2025-02-07
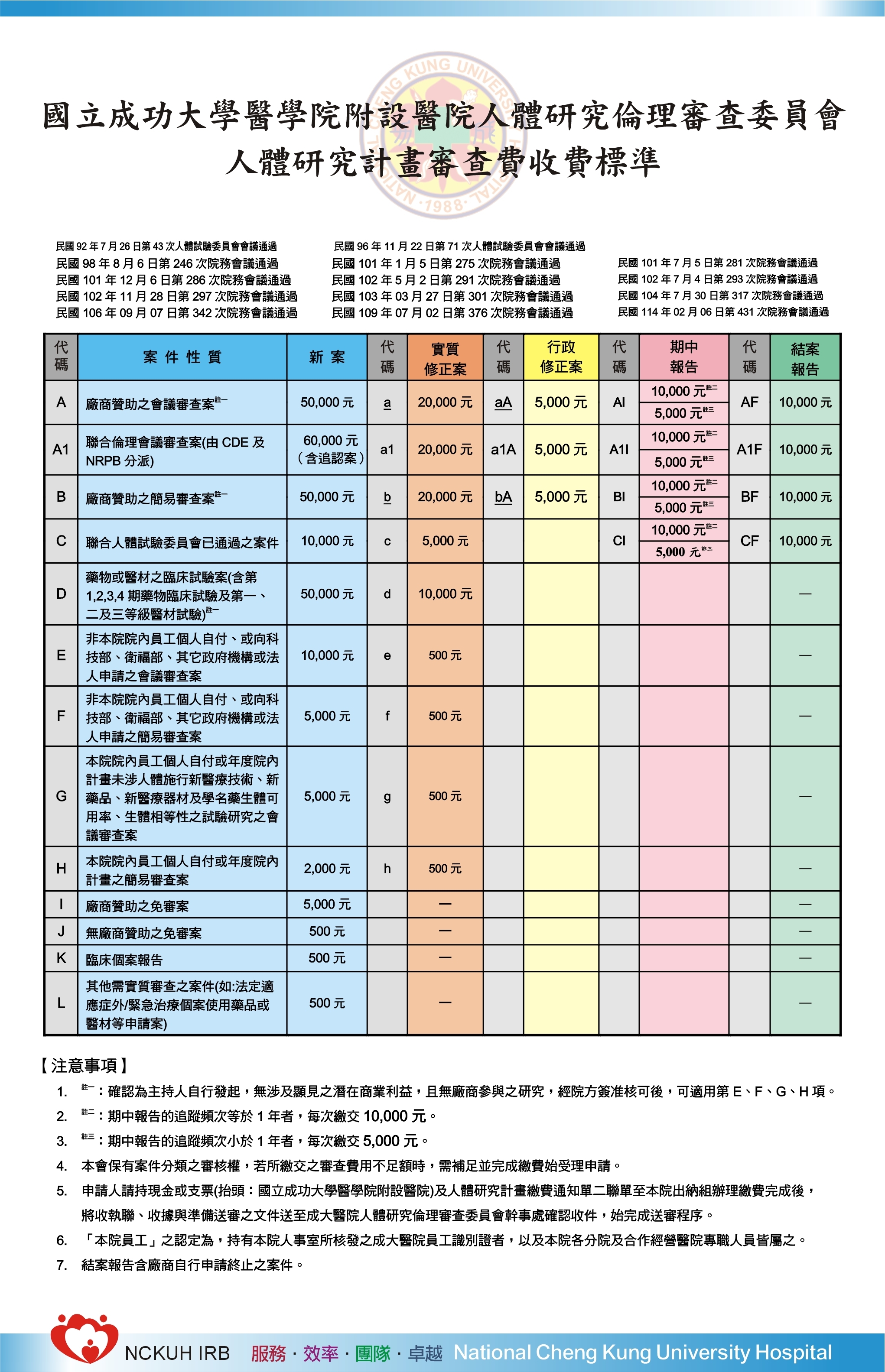
| 代碼 | 案件性質 | 新案費用 | 代碼 | 實質修正案費用 | 代碼 | 行政修正案費用 | 代碼 | 期中報告費用 | 代碼 | 結案 |
| A | 廠商贊助之會議審查案 (註一) | 50,000元 | a | 20,000元 | aA | 5,000元 | AI |
10,000元/(註二) |
AF | 10,000元 |
| 5000元(頻率小於12個月)(註三) | ||||||||||
| A1 | 聯合倫理會議審查案(由CDE及NRPB分派) | 60,000元 (含追認案) | a1 | 20,000元 | a1A | 5,000元 | A1I | 10,000元/(註二) | A1F | 10,000元 |
| 5000元(頻率小於12個月)(註三) | ||||||||||
| B | 廠商贊助之簡易審查案 (註一) | 50,000元 | b | 20,000元 | bA | 5,000元 | BI | 10,000元/(註二) | BF | 10,000元 |
| 5000元(頻率小於12個月)(註三) | ||||||||||
| C | 聯合人體試驗委員會已通過之案件 | 10,000元 | c | 5,000元 | CI | 10,000元/(註二) | CF | 10,000元 | ||
| 5000元(頻率小於12個月)(註三) | ||||||||||
| D | 藥物或醫材之臨床試驗案(含第1,2,3,4期藥物臨床試驗及第一、二及三等級醫材試驗) (註一) | 50,000元 | d | 10,000元 | - | |||||
| E | 非本院院內員工個人自付、或向科技部、衛福部、其它政府機構或法人申請之會議審查案 | 10,000元 | e | 500元 | - | |||||
| F | 非本院院內員工個人自付、或向科技部、衛福部、其它政府機構或法人申請之簡易審查案 | 5,000元 | f | 500元 | - | |||||
| G | 本院院內員工個人自付或年度院內計畫未涉人體施行新醫療技術、新藥品、新醫療器材及學名藥生體可用率、生體相等性之試驗研究之會議審查案 | 5,000元 | g | 500元 | - | |||||
| H | 本院院內員工個人自付或年度院內計畫之簡易審查案 | 2,000元 | h | 500元 | - | |||||
| I | 廠商贊助之免審案 | 5,000元 | - | - | ||||||
| J | 無廠商贊助之免審案 | 500元 | - | - | ||||||
| K | 臨床個案報告 | 500元 | - | - | ||||||
| L | 其他需實質審查之案件(如:法定適應症外/緊急治療個案使用藥品或醫材等申請案) | 500元 | - | - |
【注意事項】
- 註一:確認為主持人自行發起,無涉及顯見之潛在商業利益,且無廠商參與之研究,經院方簽准核可後,可適用第E、F、G、H項。
- 註二:期中報告的追蹤頻次等於1年者,每次繳交10,000元。
- 註三:期中報告的追蹤頻次小於1年者,每次繳交5,000元。
- 本會保有案件分類之審核權,若所繳交之審查費用不足額時,需補足並完成繳費始受理申請。
- 申請人請持現金或支票(抬頭:國立成功大學醫學院附設醫院)及人體研究計畫繳費通知單二聯單至本院出納組辦理繳費完成後,將收執聯、收據與準備送審之文件送至成大醫院人體研究倫理審查委員會幹事處確認收件,始完成送審程序。
- 「本院員工」之認定為,持有本院人事室所核發之成大醫院員工識別證者,以及本院各分院及合作經營醫院專職人員皆屬之。
- 結案報告含廠商自行申請終止之案件。

 地址:台南市704北區勝利路138號 (成大醫院門診大樓6樓IRB辦公室)
地址:台南市704北區勝利路138號 (成大醫院門診大樓6樓IRB辦公室)